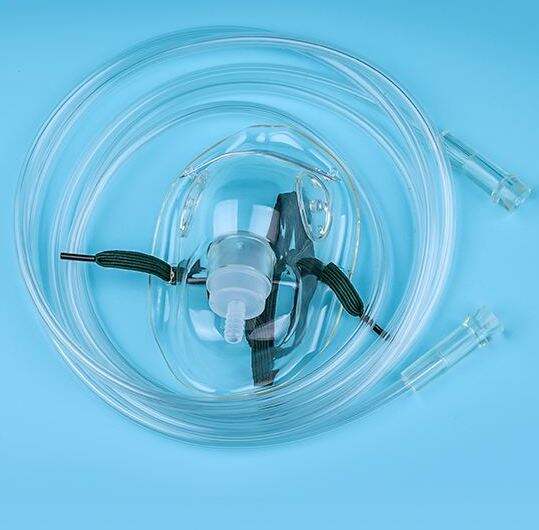
Eccellenza nella conformità normativa e nella biocompatibilità
Il quadro normativo relativo ai dispositivi medici richiede un rispetto assoluto di standard complessi e in continua evoluzione, volti a tutelare la sicurezza dei pazienti e a garantire l’efficacia del prodotto. Le parti mediche in plastica realizzate mediante stampaggio ad iniezione, prodotte attraverso processi convalidati, forniscono il percorso documentale e la tracciabilità dei materiali necessari per presentazioni normative efficaci presso enti quali la FDA, l’Agenzia europea per i medicinali (EMA) e altre autorità regolatorie internazionali analoghe. Ogni fase della produzione — dalla certificazione delle materie prime alla convalida del processo e ai test sul prodotto finito — segue procedure documentate in grado di resistere all’attento esame da parte delle autorità regolatorie. Collaborando con produttori esperti di parti mediche in plastica realizzate mediante stampaggio ad iniezione, si ottiene l’accesso a sistemi di gestione della qualità consolidati, certificati secondo lo standard ISO 13485, specificamente concepiti per la produzione di dispositivi medici. Tali sistemi garantiscono che ogni ciclo produttivo mantenga identiche specifiche tecniche, con registrazioni esaustive che tracciano i numeri di lotto dei materiali, i parametri di processo, i risultati delle ispezioni e le condizioni ambientali durante l’intero ciclo produttivo. Questa documentazione diventa estremamente preziosa durante gli audit regolatori e fornisce le prove necessarie a dimostrare la coerenza delle pratiche produttive. La biocompatibilità rappresenta un ulteriore vantaggio fondamentale delle parti mediche in plastica realizzate mediante stampaggio ad iniezione, correttamente prodotte, in particolare per i componenti che entrano in contatto diretto o indiretto con i pazienti, ad esempio tramite sostanze farmaceutiche. I polimeri per uso medico sono sottoposti a rigorosi test conformemente allo standard ISO 10993, che valutano citotossicità, sensibilizzazione, irritazione e tossicità sistemica al fine di garantire la sicurezza umana. I produttori conservano le specifiche dei materiali e i certificati di prova che ne attestano la conformità, eliminando ogni incertezza circa l’idoneità del materiale per la vostra applicazione. L’ambiente produttivo controllato per le parti mediche in plastica realizzate mediante stampaggio ad iniezione previene contaminazioni che potrebbero compromettere la biocompatibilità o introdurre particelle in applicazioni mediche sensibili. Impianti a camera pulita dotati di sistemi di trattamento dell’aria filtrata, controllo di temperatura e umidità e rigorosi protocolli per il personale garantiscono che i componenti finiti soddisfino le specifiche di pulizia essenziali per l’uso medico. Questo controllo ambientale si estende oltre la produzione alle operazioni di imballaggio, dove i componenti vengono protetti mediante materiali per imballaggi sterili o puliti, convalidati, che ne preservano la sterilità o la pulizia fino all’impiego finale. Inoltre, la costanza del materiale nelle parti mediche in plastica realizzate mediante stampaggio ad iniezione garantisce prestazioni prevedibili negli ambienti biologici, sia che i componenti siano destinati a test diagnostici, a sistemi di somministrazione di farmaci o a impieghi chirurgici. Si evita così la variabilità che può derivare da materiali lavorati con metodi meno controllati, acquisendo la fiducia che ogni componente si comporti in modo identico nelle situazioni cliniche, dove prestazioni imprevedibili potrebbero compromettere gli esiti per i pazienti.